药学系王磊副教授和美国明尼苏达大学药学院Zhengqiang Wang教授共同在国际著名期刊Accounts of Chemical Research上发表题目为“Cutting into the Substrate Dominance: Pharmacophore and Structure-Based Approaches toward Inhibiting Human Immunodeficiency Virus Reverse Transcriptase-Associated Ribonuclease H”的综述文章(DOI: 10.1021/acs.accounts.9b00450)。
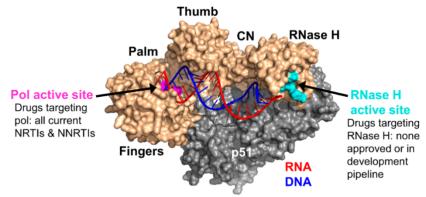
艾滋病依旧是人类难以控制的恶性传染病之一,目前所有的抗艾滋病药物都只能控制患者体内艾滋病病毒(HIV-1)的浓度,却不能彻底治愈艾滋病。自从第一例抗艾滋病药物齐多夫定被报道以来,FDA已经批准了三十多个抗艾滋病药物。虽然成果显著,但是长期服药带来的副作用和病毒耐药性的出现往往会使治疗失败。以原有靶点为基础的药物研究和作用于新靶点的药物研发有着重要的意义,尤其是后者可改善病毒耐药性,为患者提供新的药物组合。HIV-1逆转录酶是目前研究较多的一个药物靶点,可分为聚合酶功能区(Pol)和核糖核酸酶H(RNase H)功能区。聚合酶承担RNA和DNA依赖的病毒DNA聚合,而核糖核酸酶H的主要功能是从RNA/DNA逆转录中间产物中水解RNA单链。截至目前,所有的抗HIV逆转录酶药物都是作用于聚合酶区域,而以核糖核酸酶H为靶点的药物甚至还没有进入临床阶段。核糖核酸酶H作为HIV-1药物靶点的主要问题如下:1. 如何提高抑制剂对核糖核酸酶H的选择性。聚合酶功能区和核糖核酸酶H在空间和动态过程中有着紧密的相互作用,而整合酶又和核糖核酸酶有着相似的活性中心。筛选出能够选择性抑制核糖核酸酶H的化合物至关重要。2. 如何提高抑制剂的抗病毒活性。传统核糖核酸酶H抑制剂往往只能够抑制蛋白的活性,但在细胞测试中却不能表现出较好的抗病毒效果。
文章介绍了团队以核糖核酸酶H为靶点的HIV-1抑制剂的设计及相关研究工作。重点讨论基于药效团和基于结构的抗病毒药物设计理念,介绍了从最初的新型结构设计到后来开发出选择性高,抗病毒效果好的抑制剂的研发路程。研究表明:提高抑制剂的靶点选择性和细胞中的抗病毒活性,对于以核糖核酸酶H为靶点的药物研发至关重要。相关研究进一步证明将核糖核酸酶H作为新型抗HIV药物靶点有着较大的可行性和应用前景。